فشار اسمزی
بعضی از خواص محلولها اساسا به غلظت ذرات حل شده ،نه به ماهیت این ذرات بستگی دارد.این خواص را خواص غلظتی می گویند.برای محلولهای دارای مواد حل شده غیر فرار این خواص عبارتند از :کاهش فشار بخار ،نزول نقطه انجماد ،صعود نقطه جوش،و فشار اسمزی.
غشایی مانند سلوفان که برخی از مولکولها ،نه همه آنها را ازخود عبور می دهدغشای نیمه تراوا نامیده می شودشکل 1غشایی را نشان می دهدکه بین آّب خالص و محلول قند قرار گرفته است.این غشا نسبت به آب تراوا است ولی سوکروز (قند نیشکر)را از خود عبور نمی دهددر شروع آزمایش ارتفاع آب در بازوی چپ لولهU شکل برابر با ارتفاع محلول قند در بازوی راست این لوله است.از این غشا مولکولهای قند نمی توانند عبور کنند ولی مولکولهای آب در هر دو جهت می توانندعبور کنند.اما در بازوی چپ لوله(بازویی که محتوی آب خالص است)،تعداد مولکولها در واحد حجم بیش از تعداد آنها دربازوی راست است.از این رو سرعت عبور مولکولهای آّب از سمت چپ غشا به سمت راست آن بیشتر از سرعت عبور آنها در جهت مخالف است.در نتیجه تعداد مولکولهای آب در سمت راست غشا به تدریج زیاد می شود و محلول قند رقیق تر می شودو ارتفاع محلول در بازوی راست لوله زیاد می شوداین فرایند را اسمز می نامنداختلاف ارتفاع در سطح مایع در دو بازوی لوله ،اندازه فشار اسمزی را نشان می دهدبر اثر افزایش فشار هیدروستاتیکی در بازوی راست مولکولهای آب از سمت راست غشا به طرف سمت چپ آن رانده می شود تا اینکه سرانجام سرعت عبور از سمت راست با سرعت عبور از سمت چپ برابر می گردد.بنابراین حالت نهایی یک حالت تعادلی است که در آن سرعت عبور مولکولهای آب از غشادر دو جهت برابراست.اگر بر محلول بازوی راست فشاری بیش از فشار تعادلی وارد شود آب ذر جهت مخالف معمول رانده می شود .این فرایند که اسمز معکوس نامیده می شود برای تهیه آب خالص از آب نمک دار به کار می رود.بین رفتار مولکولهای آب در فرایند اسمر و رفتار مولکولهای گاز در فرایند نفوذ ،تشابهی وجود دارد در هر دو فرایند مولکولها از ناحیه غلیظ تر به ناحیه رقیق تر نفوذ می کنند
فشار اسمزی با توجه به رابطه زیر محاسبه می شود:
PV=nRT
کاربرد اسمز
اسمز در فرایندهای فیزیولوژیکی گیاهی و
حیوانی نقش دارد عبور مواد از جدار نیمه تراوا سلول زنده ،کار کلیه ها و
بالارفتن شیره گیاهی در درختان مهمترین نمونه های اسمر است.
غشای گلبولهای قرمز
از نوع نیمه تراوا است اگر گلبولهای قرمز در آب خالص قرار گیرند،آب به
درون آن نفوذ کرده و مایعات آن را رقیق می کند .در نتیجه گلبول متورم شده
وجدار آن پاره می شود واگر گلبولهای قرمز در محلول غلیظ قند قرار گیرند ،آب
درون گلبلها از غشای آنها عبور کردهو محلول اطراف آنها را رقیق می کند .در
نتیجه ،گلبولها چروکیده می شود.
به منظور ممانعت از وقوع هر یک از حوادث در تزریقات وریدی ،محلولهای مورد استفاده باید ایزوتونیک باخو ن باشند(یعنی فشار اسمزی این محلولهل باید برابر با فشار اسمزی خون باشد).
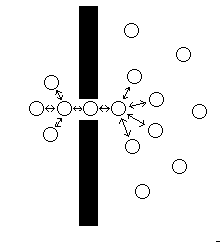
بعضی از خواص محلولها اساسا به غلظت ذرات حل شده ، نه به ماهیت این ذرات ، بستگی دارد. این خواص را خواص غلظتی (Colligative) مینامند. یکی از این خواص ، برای محلولهای دارای مواد حل شده غیر فرار ، عبارت از «فشار اسمزی» است. عامل ایجاد فشار اسمزی ، ذرات و حرکات جسم حل شونده است.
ماهیت فشار اسمزی
غشایی مانند سلوفان که برخی از مولکولها ، نه همه آنها ، را از خود عبور میدهد، غشای نیمه تراوا
نامیده میشود. غشایی را در نظر میگیریم که بین آب خالص و محلول قند قرار
گرفته است. این غشا نسبت به آب ، تراوا است، ولی «ساکارز» (قند نیشکر) را
از خود عبور نمیدهد. در شروع آزمایش ارتفاع آب در بازوی چپ لوله U
شکل برابر با ارتفاع محلول قند در بازوی راست این لوله است. از این غشا ،
محلولهای قند نمیتوانند عبور کنند، ولی مولکولهای آب در هر دو جهت
میتوانند عبور کنند.
در بازوی چپ لوله فوق (بازویی که محتوی آب
خالص است)، تعداد مولکولهای آب در واحد حجم بیش از تعداد آنها در بازوی
راست است. از اینرو ، سرعت عبور مولکولهای آب از سمت چپ غشا به سمت راست آن
بیشتر از سرعت عبور آنها در جهت مخالف است. در نتیجه ، تعداد مولکولهای آب
در سمت راست غشا بتدریج زیاد میشود و محلول قند رقیقتر میگردد و ارتفاع
محلول در بازوی راست لوله U زیاد میشود. این فرایند را اسمز مینامند.
اختلاف ارتفاع در سطح مایع در دو بازوی لوله U ، اندازه فشار اسمزی را نشان میدهد. بر اثر افزایش فشار هیدروستاتیکی
در بازوی راست که از افزایش مقدار محلول در این بازو ناشی میشود،
مولکولهای آب از سمت راست غشا به سمت جپ آن رانده میشوند تا اینکه سرانجام
سرعت عبور از سمت راست با سرعت عبور از سمت چپ برابر گردد. بنابراین حالت
نهایی یک حالت تعادلی است که در آن ، سرعت عبور مولکولهای آب از غشا در دو
جهت برابر است.
اسمز معکوس
اگر بر محلول بازوی سمت راست ، فشاری بیش از فشار تعادلی وارد شود، آب در جهت مخالف معمول رانده میشود. این فرایند که «اسمز معکوس» نامیده میشود، برای تهیه آب خالص از آب نمکدار بکار میرود.
تشابه اسمز و نفوذ
بین رفتار مولکولهای آب در فرایند اسمز و رفتار مولکولهای گاز در فرایند نفوذ ، تشابهی وجود دارد. در هر دو فرایند ، مولکولها از ناحیه غلیظتر به ناحیه رقیقتر نفوذ میکنند.
معادله وانت هوف
یاکوب وانت هوف در سال 1887 رابطه زیر را کشف کرد:
که این رابطه برای محلولهای ایدهآل میباشد. در این رابطه ، π فشار اسمزی (برحسب اتمسفر) ، n تعداد مولکولهای ماده حل شده در حجم V (برحسب لیتر) ،T دمای مطلق و R ثابت گازها (0،08206L.atm/K.mol) است. تشابه بین این معادله و معادله حالت یک گاز ایدهآل ، کاملا مشخص است. این رابطه را میتوان به صورت زیر نوشت:
که در آن M__ مولاریته محلول است. وانت هوف به خاطر این کشف ، جایزه نوبل شیمی سال 1901 را از آن خود کرد.

نقش فرایند اسمز در پدیدههای طبیعی
اسمز در فرایندهای فیزیولوژیکی گیاهی و حیوانی نقش مهمی دارد. عبور مواد از غشای نیمه تراوای سلول زنده ، کار کلیهها و بالا رفتن شیره گیاهی
در درختان ، مهمترین نمونههای اسمز است. غشای گلبولهای قرمز از نوع نیمه
تراوا است. اگر گلبولهای قرمز در آب خالص قرار گیرند، آب به درون آن نفوذ
کرده و مایعات آن را رقیق میکند.
در نتیجه گلبول متراکم شده و جدار آن پاره میشود و اگر گلبول قرمز در محلول غلیظ قند
قرار گیرند، آب درون گلبولها از غشای آنها عبور کرده و محلول اطراف آن را
رقیق میکند. در نتیجه ، گلبولها چروکیده میشوند. بمنظور ممانعت از وقوع
هر یک از این حوادث در تزریقات وریدی ، محلولهای مورد استفاده باید ایزوتونیک با خون باشد، یعنی فشار اسمزی این محلولها باید برابر با فشار اسمزی خون باشد.
 خلاصه فصل های شیمی پایه های اول و دوم و سوم وپیش دانشگاهی دوره متوسطه و خلاصه کتاب شیمی اول و دوم وسوم و پیش به همراه نمونه سوالات و مطالب جالب شیمی و همچنین شاخه های شیمی
خلاصه فصل های شیمی پایه های اول و دوم و سوم وپیش دانشگاهی دوره متوسطه و خلاصه کتاب شیمی اول و دوم وسوم و پیش به همراه نمونه سوالات و مطالب جالب شیمی و همچنین شاخه های شیمی